Abstract
Le Neoplasie Peritoneali si sviluppano frequentemente nella storia naturale di molti tumori rappresentando uno dei maggiori problemi di gestione oncologica. I rari tumori primitivi del peritoneo di cui i Mesoteliomi Peritoneali sono i più frequenti così come le Carcinosi Peritoneali sono spesso associati a gravi problemi clinici per il paziente. Considerati in passato delle condizioni terminali, le Neoplasie del Peritoneo sono state trattate nelle ultime due decadi quali malattie curabili. L’introduzione nella pratica clinica da parte di Sugarbaker della Citoriduzione Chirurgica/Peritonectomia nel trattamento delle neoplasie peritoneali e la diffusione della metodica nell’ambito della comunità scientifica ha drasticamente cambiato la storia naturale di tali patologie. Un’altra metodica che ha dimostrato un importante impatto nel controllo delle neoplasie peritoneali è la Chemio Ipertermia Intra Peritoneale. E’ certamente una delle aree di ricerca che in atto suscita particolare interesse nell’ambito della comunità scientifica sia per l’impatto sulla sopravvivenza che sulla qualità di vita dei pazienti trattati con un modesto costo in termini di morbilità e mortalità. L’obiettivo di questo lavoro è quello di illustrare il razionale, le tecniche ed i risultati dell’approccio multimodale alle Neoplasie Peritoneali mediante la Citoriduzione Chirurgica/Peritonectomia associata alla Chemio Ipertermia Intra Peritoneale.
Premessa
La Carcinosi Peritoneale (CP) è un evento prognosticamente sfavorevole che caratterizza in particolare l’evoluzione delle neoplasie degli organi a sede addomino-pelvica potendo in misura minore presentarsi quale stadio terminale di neoplasie extra-addominali ( 1,2 ,3 ). Il concetto che ad una diagnosi di CP si associ una prognosi severa per il paziente è ampiamente diffuso nell’ambito della comunità scientifica. L’indicazione stessa di un trattamento chirurgico di un tumore primitivo gastrointestinale è fortemente influenzata dalla presenza di CP. Ciò perché, per lungo tempo la CP è stata considerata una patologia non suscettibile di un trattamento curativo ed in particolare di un intervento chirurgico. Le motivazioni sono varie. Il peritoneo non è infatti considerato un organo, ma semplicemente un foglietto che riveste la cavità addominale e gli organi che vi sono alloggiati; eppure ha una struttura istologica, una vascolarizzazione, una disposizione e soprattutto una funzione. Parimenti al fegato ed al polmone, è soggetto a metastatizzazione da parte di molti tumori ed in particolare quelli originati dagli organi contenuti nella cavità addominale. Come qualunque altro organo inoltre, può essere sede di un tumore primitivo,anche se raro, definito Mesotelioma Peritoneale e di altri tumori più rari di origine non mesoteliale. La sua disposizione è complessa; i suoi 7.600 cm2 si distribuiscono infatti con una disposizione complessa tale da consentire rapporti con tutte le strutture che sono contenute o transitano nell’addome; tale disposizione tuttavia rende complessa anche la distribuzione di una neoplasia peritoneale, primitiva o secondaria, che andrà inevitabilmente a seguire l’anatomia del peritoneo. L’evoluzione delle tecniche chirurgiche e la disponibilità di presidi terapeutici innovativi in ambito chirurgico ed anestesiologico hanno consentito di applicare un trattamento chirurgico anche al peritoneo. La CP è stata ed in gran parte è tuttora trattata mediante Chemioterapia (CT) sistemica eventualmente associata ad interventi di debulking chirurgico con l’obiettivo di ridurre la massa e migliorare la sintomatologia.
Nel 2000, è stato pubblicato un articolato lavoro riguardante uno studio prospettico multicentrico sulla CP (EVOCAPE 1) (4) che ha coinvolto 9 centri universitari ed ospedalieri francesi, con un reclutamento nel ’95-’97. Lo studio ha arruolato 125 pazienti con CP da carcinoma gastrico, 118 da carcinoma del colon, 58 da carcinoma del pancreas variamente distribuiti per stadio (0= no macroscopica evidenza, I < 5mm localizzato, II < 5mm diffuso, III 5-20mm, IV > 20mm) e sottoposti ad interventi palliativi e/CT. La sopravvivenza mediana è stata fortemente influenzata dal tipo istologico del tumore primitivo essendo di 3.1, 5.2, 2.1 mesi rispettivamente per carcinoma dello stomaco, del colon e del pancreas. Se consideriamo il sottogruppo dei 118 pazienti con CP da carcinoma colorettale, il 60% della casistica presentava noduli di diametro <2cm; tuttavia quando trattati senza intento curativo hanno evidenziato una sopravvivenza limitata. Queste considerazioni note da tempo e confermate in questo recente lavoro, hanno indotto molti ricercatori a sviluppare studi mediante l’utilizzo di metodiche innovative per il trattamento della CP. Un trattamento che ha sicuramente contribuito al miglioramento della sopravvivenza dei pazienti affetti da CP consiste nella strategia terapeutica locoregionale.
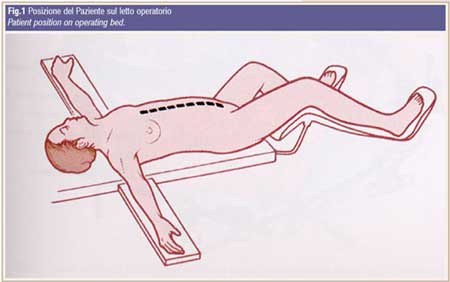
Principi della metodologia
Approccio locoregionale delle malattie neoplastiche del peritoneo
L’approccio innovativo mediante la combinazione tra la chirurgia citoriduttiva (CCR) e la chemioipertermia intraperitoneale (CIIP), trova il suo razionale nella caratteristica storia naturale della CP. Nel carcinoma ovarico ed in una elevata percentuale di carcinoma del colon, la malattia rimane confinata all’addome per gran parte della sua storia naturale, conferendone una caratteristica evoluzione loco-regionale. Questa è la caratteristica biologica che ha consentito l’opportunità di un approccio selettivo, quale il trattamento chemioterapico intraperitoneale. L’elevata concentrazione di farmaco ottenibile mediante un trattamento locoregionale, consente infatti di superare la resistenza intrinseca od acquisita nei confronti del farmaco e simultaneamente ridurre gli effetti collaterali sistemici.
Il razionale della CIIP
Il concetto fondamentale di un trattamento intraperitoneale è rappresentato dalla tendenza di alcuni farmaci a concentrarsi a livello del peritoneo attraversandolo solo gradualmente. Tale probabilità dipende da molteplici fattori, tra cui la supposta presenza di una barriera Plasmatico-Peritoneale. Tale ipotesi è basata su diversi studi che confermano l’esistenza di un gradiente plasmatico-peritoneale. La barriera è rappresentata dal tessuto sottomesoteliale e dalla membrana basale dei capillari, che limitano il riassorbimento di farmaci idrofili o ad elevato peso molecolare come la mitomicina C, il cisplatino e la doxorubicina. È stato dimostrato che il cisplatino ha una maggiore capacità di penetrazione nel tessuto tumorale quando somministrato in condizioni ipertermiche. Inoltre, a 40-42 C le cellule neoplastiche diventano più chemiosensibili per l’aumentata concentrazione intracellulare dei farmaci, la maggiore attivazione, specialmente per gli agenti alchilanti,la diminuita capacità di riparo dei danni al DNA. Questi eventi sono più intensi nelle cellule tumorali ovariche cisplatino-resistente che nelle cellule cisplatino-sensibili (5).
La formazione di addotti platino-DNA dopo esposizione al cisplatino è aumentata e la sua rimozione ridotta in condizioni ipertermiche, con un conseguente relativo effetto letale sulle cellule.
Analogo comportamento in condizioni di ipertermia è tipico di altri farmaci e come la Doxorubicina e la Mitomicina C.
Descrizione della tecnica(6)
Citoriduzione chirurgica
Il concetto di chirurgia citoriduttiva (CCR) deve essere inteso come completa asportazione degli impianti neoplastici con eventuali microresidui di dimensioni non superiori a 2,5 mm (target ottimale della CIIP).
La metodica necessita di regola di manovre di peritonectomia secondo la tecnica descritta da Sugarbaker (7)Un dispositivo chiamato ball-tip electrosurgical handpiece mediante uno elettrodo sferico di 2 mm viene utilizzato per dissecare il peritoneo tumorale della parete addominale normale. Verrà utilizzato il bisturi elettrico ad alto voltaggio.
Fase chirurgica
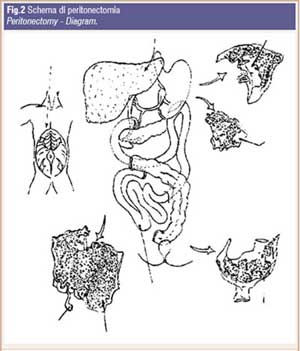
La CCR viene ottenuta mediante una sequenza ordinata di manovre ben codificate che vengono eseguite in funzione dell’estensione della malattia (Fig.2):
- Resezione del grande omento, peritonectomia parietale destra resezione del colon destro;
- Peritonectomia del quadrante superiore sinistro e parietale sinistra, splenectomia;
- Peritonectomia del quadrante superiore destro, resezione della capsula Glissoniana, peritonectomia della tasca di Morrison;
- Resezione del piccolo omento, citoriduzione dell’ilo epatico ± colecistectomia, ± resezione parziale o totale dello stomaco
- Peritonectomia pelvica ± resezione del sigma ± isterectomia ed annessectomia bilaterale;
- Altre resezione intestinali e/o resezioni di massa tumorale;
- Anastomosi intestinali.
Chemioipertermia intraperitoneale
Dopo la citoriduzione, 4 cannule vengono posizionate nella cavità addominale. Due di queste verranno utilizzate per l’infusione del liquido, rispettivamente nella cavità sottofrenica destra e nella pelvi. Le rimanenti due cannule verranno posizionate rispettivamente nella cavità in sede centro addominale e superficialmente nella pelvi per la effusione del liquido (fig. 3).
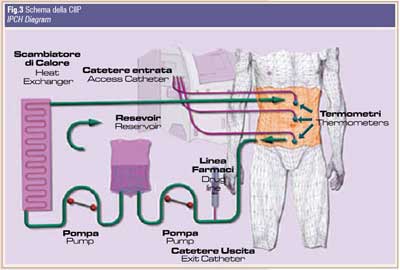
Macchina per CEC e circuito
La perfusione peritoneale prevede l’utilizzazione di una macchina che presenti le seguenti peculiarità:
1) un sistema di pompe;
2) un termostato o scambiatore di calore;
3) sistemi integrati di controllo delle temperature, delle pressioni e del flusso;
4) sistema di analisi dei dati mediante uno specifico programma computerizzato con visualizzazione in tempo reale dei parametri e loro registrazione;
5) un circuito extracorporeo (CEC). L’apparecchiatura deve essere garantita dalla normativa C.E. Vengono inoltre utilizzati una serie di termometri per la valutazione costante della temperatura intraaddominale. Molti centri attivi, in atto utilizzano l’apparecchiatura Performer LRT (fig. 4).
Priming
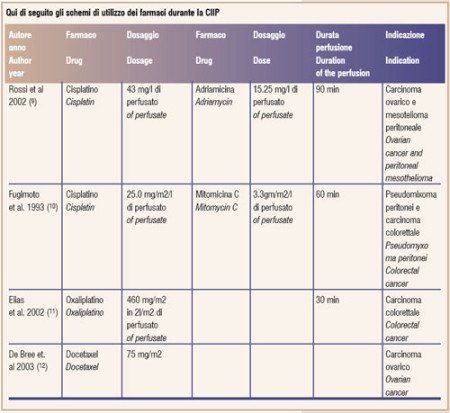
 Per priming si intende il liquido di riempimento del circuito. All’Istituto Tumori di Milano è stata sperimentata una soluzione composta per 2/3 da soluzione Normosol R pH 7.4 e per 1/3 da Emagel. Per quanto riguarda il volume ottimale del priming questo deve essere sufficientemente abbondante ai fini di garantire una temperatura omogenea e constante, ma non eccessivo al punto di causare una distensione addominale e termodiluzione corporale. Pertanto, per un adeguato funzionamento del circuito un volume di 3 a 4 litri per la tecnica ad addome aperto e 6 litri per la tecnica ad addome chiuso sono sufficienti (8). Nella tecnica ad addome chiuso, la pelle della parete addominale è temporaneamente chiusa con sutura continua e le cannule vengono connesse al circuito ai fini di iniziare la CIIP. Nella modalità aperta, l’addome è coperto con uno strato di materiale plastico ed il vapore dei farmaci sono aspirate per proteggere l’equipe della sala operatoria. Il perfusato riscaldato contenente i farmaci viene somministrato nella cavità peritoneale attraverso la macchina con un flusso medio di 600-1000 ml/min per 60/90 minuti. Al fini di ottenere una temperatura intra-addominale di 42.5 C, è necessario mantenere la temperatura di infusione a 44 C circa. Durante la perfusione, se la tecnica in utilizzo è ad addome aperto, l’operatore deve continuamente manipolare l’intestino al fini di garantire una omogenea distribuzione di calore e chemioterapici. Dopo la perfusione, il perfusato viene rapidamente drenato e si procede la chiusura della parete addominale dopo un’ispezione accurata della cavità.
Per priming si intende il liquido di riempimento del circuito. All’Istituto Tumori di Milano è stata sperimentata una soluzione composta per 2/3 da soluzione Normosol R pH 7.4 e per 1/3 da Emagel. Per quanto riguarda il volume ottimale del priming questo deve essere sufficientemente abbondante ai fini di garantire una temperatura omogenea e constante, ma non eccessivo al punto di causare una distensione addominale e termodiluzione corporale. Pertanto, per un adeguato funzionamento del circuito un volume di 3 a 4 litri per la tecnica ad addome aperto e 6 litri per la tecnica ad addome chiuso sono sufficienti (8). Nella tecnica ad addome chiuso, la pelle della parete addominale è temporaneamente chiusa con sutura continua e le cannule vengono connesse al circuito ai fini di iniziare la CIIP. Nella modalità aperta, l’addome è coperto con uno strato di materiale plastico ed il vapore dei farmaci sono aspirate per proteggere l’equipe della sala operatoria. Il perfusato riscaldato contenente i farmaci viene somministrato nella cavità peritoneale attraverso la macchina con un flusso medio di 600-1000 ml/min per 60/90 minuti. Al fini di ottenere una temperatura intra-addominale di 42.5 C, è necessario mantenere la temperatura di infusione a 44 C circa. Durante la perfusione, se la tecnica in utilizzo è ad addome aperto, l’operatore deve continuamente manipolare l’intestino al fini di garantire una omogenea distribuzione di calore e chemioterapici. Dopo la perfusione, il perfusato viene rapidamente drenato e si procede la chiusura della parete addominale dopo un’ispezione accurata della cavità.
Periodo post-operatorio immediato.
Nel periodo post-operatorio i pazienti sottoposti a CCR + CIIP vengono assistiti presso l’unità di terapia intensiva per un periodo di circa 72 ore. I pazienti ricevono un trattamento con plasma fresco congelato in quantità tale da mantenere adeguato il livello serico di albumina. Al fine di prevenire un’ eventuale insufficienza renale, i pazienti vengono adeguatamente idratati. Inoltre, sono attentamente valutati i parametri emodinamici, di funzionalità renale ed epatica.
Patologie bersaglio
- CP resecabile da carcinoma dell’ovaio (17,88,18)
- Mesotelioma peritoneale (19,20)
- CP resecabile da carcinoma colorettale (21,22,23,24,25)
- Tumori mucinosi dell’appendice condizionanti un Pseudomixoma peritonei (26,27)
- Carcinomi dell’appendice con CP resecabile (28)
- Carcinoma dello stomaco con CP resecabile (29,30,31,32)
Elegibilità
Criteri di inclusione
- età inferiore ai 75 anni;
- adeguata funzionalità renale, epatica e midollare;
- performance status (ECOG) 0, 1 or 2;
- consenso informato firmato dal paziente.
Criteri di Esclusione
- impossibilità di un adeguato follow-up;
- presenza di altre malattie neoplastiche maligne;
- infezione attiva o altre condizione cliniche contemporanee che possano interferire nella capacità del paziente di ricevere il trattamento proposto secondo il protocollo;
- metastasi extradistrettuali;
- occlusione intestinale completa.
- inadeguata funzionalità renale, epatica o midollare.
Stato dell’arte
Carcinoma del colon
Interessanti risultati sono stati recentemente pubblicati da Glehen (23) riguardanti uno studio retrospettivo condotto su 506 pazienti sottoposti a peritonectomia e CIIP; a questo studio hanno concorso i più importanti centri italiani. La sopravvivenza mediana globale è stata di 19,2 mesi; i pazienti che hanno ottenuto una citoriduzione completa, hanno avuto una prognosi migliore con una sopravvivenza mediana di 32,4 mesi. La completezza della citoriduzione si è rivelata essere una variabile statisticamente significativa (p< .001)
Infine, Verwaal- Zoetmuller e collaboratori. (25) hanno condotto uno studio prospettico in cui 105 pazienti affetti da CP da carcinoma colorettale sono stati randomizzati. Il braccio sperimentale prevedeva la CCR associata alla CIIP, seguita da chemioterapia sistemica mentre il braccio controllo prevedeva la terapia standard con chemioterapia sistemica (5-fluorouracile-leucovorin) con o senza chirurgia palliativa. Il gruppo sperimentale ha presentato un vantaggio di sopravvivenza significativo rispetto al gruppo controllo.
Carcinoma gastrico
Recentemente sono stati pubblicati i dati di un trial randomizzato prospettico su 248 pazienti affetti da carcinoma gastrico, nei quali la CIIP era stata associata alla chirurgia tradizionale; i risultati della sopravvivenza a distanza sono stati statisticamente significativi per le neoplasie avanzate, con sopravvivenza a 5 anni del 49% nei pazienti sottoposti a CIIP associata a chirurgia rispetto al 18% nei pazienti con sola chirurgia (29).
E’ quindi fortemente ipotizzabile un miglioramento nelle incidenze delle recidive locali e delle sopravvivenze globali nel cancro dello stomaco avanzato, associando asportazione di organo, peritonectomia distrettuale e chemioterapia locoregionale.
In definitiva siamo di fronte ad una rivoluzione di pensiero: se le carcinosi peritoneali non sono più considerate malattie sistemiche incurabili, la peritonectomia associata a chemioterapia intraperitoneale ed ipertermia ne rappresenta la risposta terapeutica più razionale e moderna.
Carcinoma ovarico
Un importante studio di fase II è stato condotto dalla SITILO su 27 pazienti con tumore epiteliale dell’ovaio avanzato, confermato istologicamente e sottoposte a Peritonectomia + CIIP (18). Tutte le pazienti presentavano malattia ricorrente o progressiva in seguito a Chirurgia di stadiazione e chemioterapia sistemica. Le pazienti presentavano una età media di 53 anni (30-67); il follow-up medio è stato di 17.4 mesi (0.3-36). Dopo l’intervento di citoriduzione e d’accordo con i criteri descritti precedentemente, 15 (55%), 4 (15%) 3 (11%)e 5 (19%) delle pazienti, presentavano rispettivamente una completezza di citoriduzione CC-0, CC-1, CC-2; e CC-3. La sopravvivenza globale (SG) a due anni per la serie globale di pazienti è stata del 55%. La sopravvivenza libera da malattia e la sopravvivenza libera da malattia locoregionale per lo stesso periodo sono state del 21% e 44% rispettivamente. Le variabili che hanno influenzato significativamente la SG sono state la radicalità della citoriduzione, l’estensione della carcinomatosi, l’età delle pazienti e l’intervallo tra la diagnosi e la terapia con CCR+CIIP. Il volume di malattia residua ha influenzato significativamente la sopravvivenza globale (SG) (P=0.00025). Pazienti con malattia residua microscopica o minima (CC-0/1) hanno avuto il 77% di probabilità di sopravivenza a due anni (mediana 20,3 mesi), mentre tutte le pazienti con malattia residua >2.5mm (CC-2/3) sono decedute entro 20.3 mesi (mediana 4,3 mesi). Riguardo l’estensione della malattia, pazienti con carcinosi P1/P2, hanno dimostrato soltanto una tendenza ad una sopravvivenza più lunga rispetto al gruppo P3 (SG a due anni- 63% vs 50%, P=0.09). Altro fattore correlato con la SG è stato l’età. Il gruppo di pazienti con età superiore a 53 anni hanno presentato 67% di SG a due anni, mentre il gruppo con età inferiore ha avuto un andamento prognostico più sfavorevole con una SG a due anni del 40% (P=0.04).
Pseudomixoma Peritonei
In considerazione della rarità di incidenza di questa patologia, non vi sono molti studi pubblicati in letteratura ,se si escludono i cosiddetti case report. Una delle più importanti casistiche pubblicate, riguarda uno studio multicentrico condotto dalla SITILO (27). Sono stati complessivamente inclusi nello studio 70 pazienti (31 maschi e 39 femmine) di età media di 56 anni (range: 24 a 76). Un’ ottimale citoriduzione è stata ottenuta nell’ 87% dei pazienti. La morbilità post-operatoria grado III è stata del 14%; un paziente è deceduto 30 giorni dopo il trattamento per emorragia e complicanze conseguenti ad una fistola duodenale. La tossicità correlata alla CIIP è stata del 9%. Il follow-up medio è di 28.6 mesi (range: 2-72). A 5 anni, la sopravvivenza globale è stata del 91%, l’intervallo libero da progressione 54% ed un controllo locale della malattia è stato ottenuto nel 69% dei pazienti.
Mesotelioma Peritoneale
La casistica più numerosa pubblicata in letteratura scientifica e riguardante il trattamento di peritonectomia associato a chemio-ipertermia-intra-peritoneale riguarda un lavoro multicentrico condotto dalla SITILO: 61 pazienti (31M, 30F) di età compresa tra 24-72 anni (media: 51) affetti da MP, sono stati sottoposti a Peritonectomia+CIIP ±CT (25).
La comparsa di ascite, massa addominale o l’incremento del marcatore tumorale è stato considerato segno di progressione. Studi bio-molecolari e di farmacologia preclinica sono stati condotti su materiale prelevato al momento della CCR (19 e 7 casi, rispettivamente). Una soddisfacente peritonectomia è stata possibile nel 74% dei pazienti, che alla fine dell’intervento risultavano radicalmente citoridotti oppure presentavano un residuo <2,5 mm. Il follow-up medio è attualmente di 20 mesi.
Con questo regime terapeutico, la probabilità di sopravvivenza globale a 5 anni è del 54% e la sopravvivenza libera da progressione del 37%.
dr. Marcello Deraco
Surgeon, Oncologist,
Responsable, Peritoneal Neoplasia,
Program, “National Institute Tumors”, Milan, Italy






